|
※ 감수인 의견 아델릭스 소개할 때부터 느낀 벽인데요. 바이오 산업은 엄청난 모멘텀이 있는 회사들이 많고, 저는 그 분야에 대한 투자를 거의 하지 않아서 지식이 많이 부족합니다. 저자의 글을 읽으면서 느낀 점은 실패를 조금만 줄여도 아웃풋이 클 수 있겠다는 생각이 듭니다. 투자적으로 말씀드리면, 이렇게 모멘텀이 큰 회사 10개 정도 보유하면, 한 두개만 성공해도 나머지에서 실패한 손실을 다 메우고도 남을 듯 합니다 (벤처에 투자하는 손정의식 투자와 유사합니다).
대부분의 독자가 잘 모른다고 여기고, 같이 공부할겸 용어 검색 결과 드립니다. Unmet medical needs : 치료법이 없거나, 있지만 적절하지 않은 경우 *앱을 설치하시면, 구독하시는 크리에이터에 대한 새글 알림을 받아보실 수 있습니다. 지속 개선 중. '오렌지보드' 로 검색하셔서 설치 부탁 드립니다. |
바이오투자는 High Risk, High Return 입니다. 그래서 바이오투자를 도박에 비유하는 사람도 있고, 못믿을 투자라고 보는 분들도 계십니다.
하지만 바이오산업은 고령화사회로 나아가는 현시점에서, 그리고 인간은 보다 더 건강한 삶을 누리려는 욕구로 인해 결코 사양산업이 될수 없는 산업니다.
그렇다면 바이오투자에 접근하면서, High Risk를 조금이라도 경감시킬 수 있는 방법이 있으면 좋을텐데, 이런 방법을고민하다 다음과 같이 종목을 발굴하고 있다는 것을 얼마전 아델릭스(ARDX) 종목 분석 글을 통해 말씀드린 바 있습니다.
다시 요약해보자면
1. CRL 등으로 폭락한 주식
2. 임상에 문제 없어야할 것 (안전성, 효능)
3. 크던 작던 매출이 발생한 회사
4. unmet medical needs
5. (1,2)번과 연결되지만, 임상은 성공하고 허가전 단계
(즉 롱텀한 기다림이 있어야할 주식 제외, 임상리스크 제외)
이런 발굴 방법을 통해 오늘 분석할 회사는 프로탈릭스 바이오테라퓨틱스 (티커: PLX) 입니다.

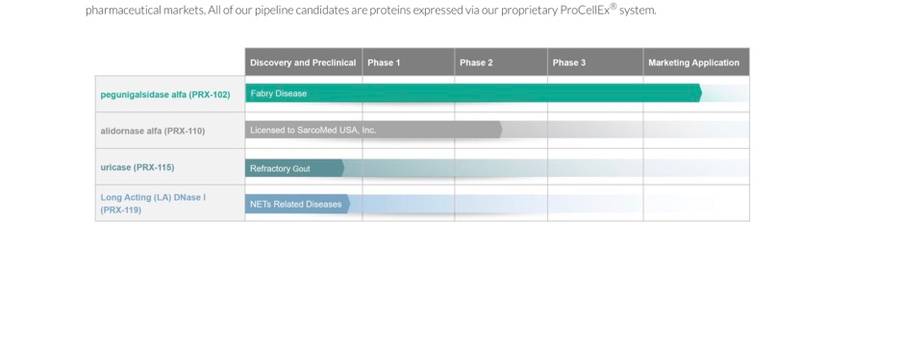
이 회사의 주요점이 잘 요약되어 있는 슬라이드입니다.
아델릭스처럼 이 회사도 이미 fda 승인받아 시판중인 약물이 있습니다.
Eleyso라는 상품명이고, 희귀질환인 고셔병치료제이고, 화이자에 라이센싱되어 판매되고 있습니다.
현재 이 회사의 가장 하이라이트되는 부분은 PRX 102 파이프라인이고, 휘귀 유전질환인 패브리병 치료제입니다.
현재 유럽 EMA의 자문위원회에선 승인권고를 받은 상태이고, 5월 초 (5월2일 예상)쯤 EMA 승인여부가 결정될 예정입니다. 미국 FDA에도 올해 5월 9일 PDUFA가 예정되어 있습니다.
즉 주요 catalyst가 코앞에 와있는 상황이죠.
PRX102는 Chiesi라는 이탈리아 글로벌제약회사에 라이센싱이 되어 있습니다. 참고로 Chiesi는 천식흡입기로 유명한 글로벌 회사 중 하나입니다.
프로탈릭스는 또한 고유의 플랫폼을 가지고 있습니다. ProCellEx라는 플랫폼인데 cGMP 제조시설을 보유하고 있고, FDA와 EMA에 이미 성공적인 오딧을 하였습니다.
이제 조금씩 더 자세히 알아볼텐데요. 아무래도 파이프라인에 더 공부해보기 전에 프로탈릭스가 보유한 플랫폼에 대해서 조금 더 알아보겠습니다.

ProCellEx 플랫폼은 식물기반 세포생산 플랫폼입니다.
보통 mammalian(포유류) cell expression 방식이나 박테리아와 효모 cell expression 방식 등이 있는데, 이런 부분보다 식물기반 세포생산시스템의 장점은
1.포유류 성분으로 인한 바이러스 오염우려가 적음
2.상온에서 유지 및 제조 가능하단 점
3.빠른 제품생산과 출시가 가능하단 점
4.사용 및 유지관리가 편하단 점
그에 반해 Mammalian은 바이러스 오염우려가 있고, 박테리아 와 효모 방식은 간단한 단백질생산만 가능하고 항체나 엔자임 등 다른 복잡한 단백질 생산은 불가능하다고 합니다.

이런 식물기반 플랫폼을 통해 프로탈릭스는 이미 시판된 약물이 있습니다. 고셔병 치료제로 Eleyso 라고 합니다.
Fda에 승인받은 최초의 식물세포 유래 재조합 단백질 약물이라고 하네요
2009년에 전세계 독점권 라이센싱을 화이자와 계약맺었고, 2015년에 브라질은 제외하는 걸로 개정하였습니다. 즉 브라질에서의 수입은 프로탈릭스의 직접적인 자금원이되고, 브라질 외 다른 세계에서는 화이자에 로열티를 받는 구조입니다.
위 Eleyso는 프로탈릭스의 ProCellEx 플랫폼이 검증되었단 걸 의미하기도 하고, 프로탈릭스로서 든든한 자금원이 되고 있는데, (하지만 아직 적자) 22년도에 브라질에서 7.2m달러 (약 93억원)의 매출을 올리고 있고, 25%의 마켓쉐어를 유지하고 있으며, 매년 10%이상의 성장이 예상된다고 합니다.
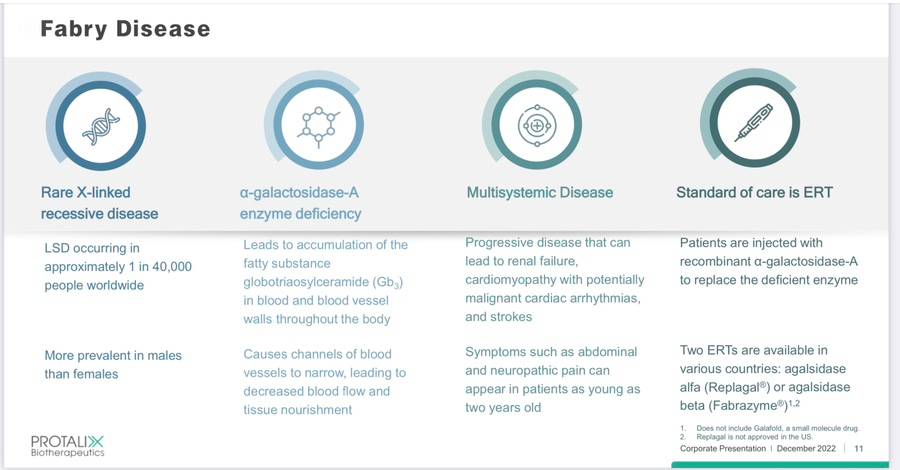
본격적으로 메인 파이프라인인 PRX102를 얘기하기 앞서서 패브리 병에 대해서 알아봐야 하는데,
패브리병은 희귀질환이며, 전세계적으로 4만명 당 1명에서 발생하는 유병율을 보이고 있고, 여성보다 주로 남성에서 발생합니다.
패브리 병은 a-galactosidase-A효소의 결핍 때문에 발생하는데, 전신의 혈액과 혈관벽에 Gb3가 축적이 되어 혈관통로가 좁아지고, 조직에 영양이 줄어듭니다.
그렇기때문에 전신성 질환이라고 보면되고, 질환이 진행됨에 따라 신부전, 심부정맥을 동반한 심근병증, 뇌졸중 등으로 이어질수 있고, 증상은 2살 어린 아기에게도 신경병증성 통증이나 복통이 나타날수가 있다고 합니다.
현재 치료는 결핍된 효소를 대체하기 위해 재조합된 a-galactosidase-A를 주사하는 ERT요법으로 치료되고 있습니다. 현재 여러나라에서 시판된 ERT 치료제는 2개가 있는데,
agalsidase alfa는 Replagal이란 상품명이고 타케다가 팔고 있으며, agalsidas beta는 Fabrazyme이란 상품명으로 사노피에서 판매하고 있습니다.
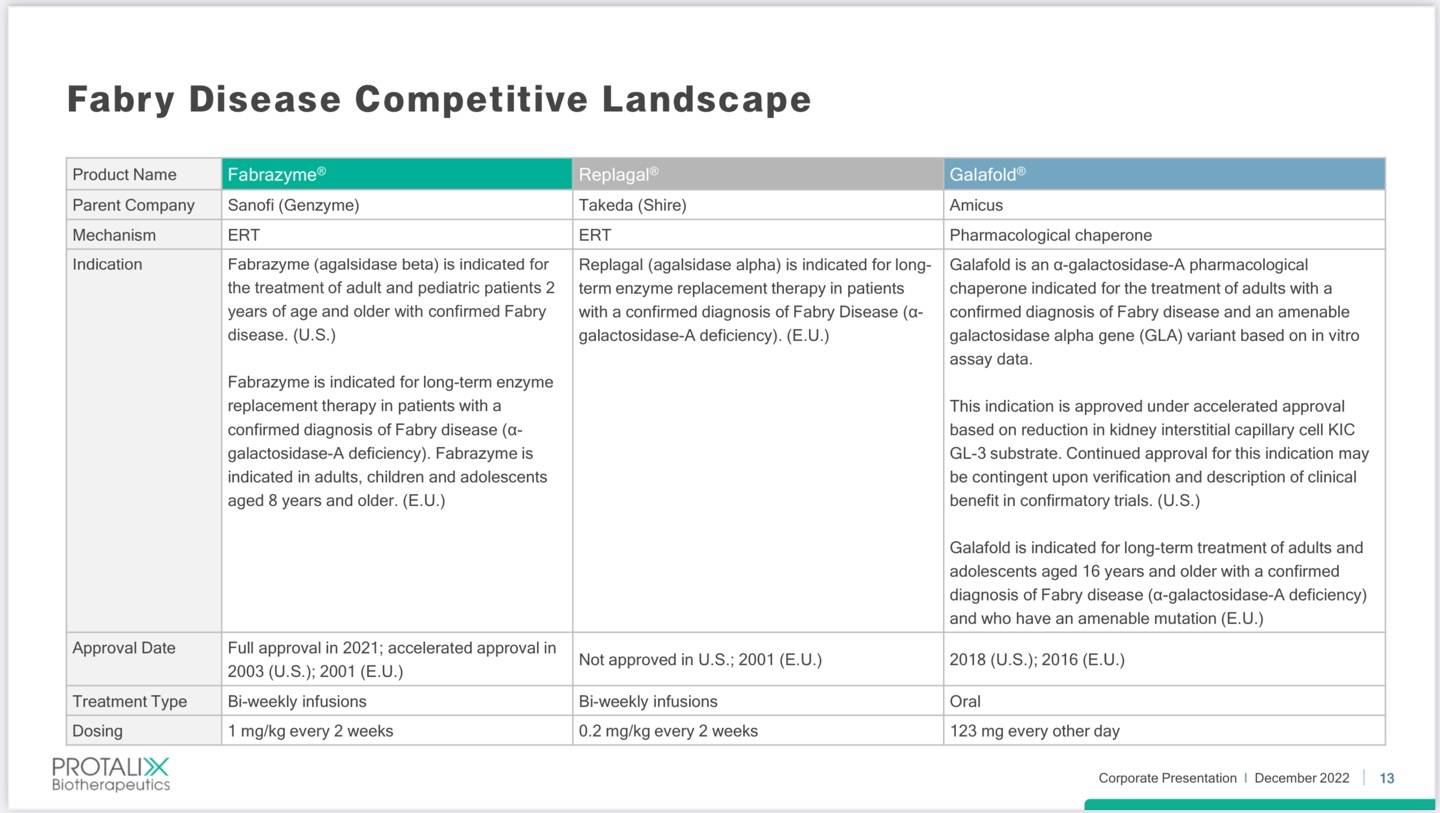
주요 경쟁품은 위에서 설명한 2개인데, 그중에서도 최근에 승인받은 Fabrizyme이 주요 경쟁자로 보면 될것 같네요

PRX102(성분명: Pegunigalsidase Alfa)는 패브리병에서 상당한 잠재력이 있다고 하는데요
유병율이 4만명 중 1명인 시장에서 환자들은 일반적으로 부족한 효소를 대체하기위해 정기적이고 롱텀한 치료법이 필요한 상황이고, 현재 ERT치료받는 환자들은 항약물 항체가 생기거나 infusion-related reaction을 경험하고 있는 상황입니다. (뒤에 설명할테지만 이 부분에 PRX 102가 가진 장점이 있습니다)
글로벌 마켓으로 본다면, 21억달러(2조7천억원) 이상의 시장이고, 27년까지 매년 10% 성장이 예상되고 있고, PRX102 런칭시 글로벌 ms 20~25% 예상된다고 합니다.
위에 언급했듯 이미 Chiesi에 라이센싱되어 있어 로열티가 발생하는데, 로열티 계약이 잘 되어 있어,
잠재적으로 연 150m~200m (2000억원~2500억원) 로열티수입이 발생할거라고 생각하고 예측되고 있습니다.
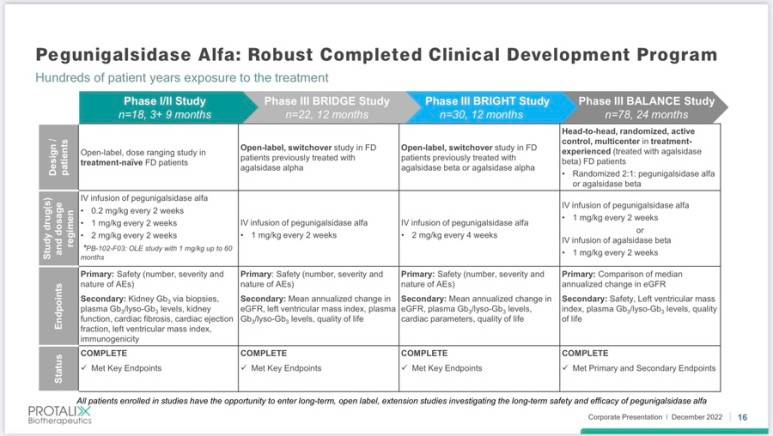
PRX102의 임상결과들을 보도록 하면,
희귀질환이다보니 환자수는 많지 않지만, 3상임상을 3개를 진행했고, 모두 임상이 성공했습니다.
(아델릭스의 경우도 마찬가지였죠. 3개임상 모두 성공)
그 중에서 3개의 3상 임상을 보면,

Bridge 스터디와 Bright 연구에선 혈장 Gb3의 개선이 이루어졌고, eGFR 기울기의 개선이 이뤄진 것을 확인할 수 있었고, Balance 연구에선, 현재 시판중인 사노피의 agalsidase beta 와 비열등성 임상을 진행했고, 사노피의 약물과 비교했을때 열등하지 않음을 입증했습니다. (head to head 연구에선 주로 비열등성 시험을 합니다)

3개의 3상 연구에서 안전성 데이터를 보면 모두 안전성을 입증했고,특히 head to head 연구를 했던 Balance 연구에서 사노피의 치료제 대비 저 적은 이상반응을 보였고,
특히 ERT요법의 주요 문제점중 하나인 infusion-related reaction에선 확연히 나은 모습을 보였습니다.

현재 3가지 연구 모두 오픈라벨로 확장스터디를 진행하고 있는데, 여기서 지켜봐야 할 부분은
Bright연구에서는 kg당 2mg으로 매 4주간 투약 팔로업입니다 (연장전 기존스터디에서도 그랬음)
해당연구에서도 이미 효능을 보았지만 4주간격 장기 투약으로 효과와 안전성이 괜찮으면 4주투약법으로 허가받을 수 있는 것이고, 이건 기존의 다른 약들이 2주간격이였던 것보다 텀이 길어지니 환자들에게도 확실한 베네핏이 될수 있을 것으로 보여집니다. 다만 현재 2주 간격으로 투약으로 승인받을 가능성이 높아보이고, 라벨링 확장은 승인 및 시판후에 이뤄질수도 있습니다.

매년 꾸준히 연구성과를 보여왔고, 22년에 EMA와 FDA에 BLA를 신청했고, 올해 상반기에 결과가 나올것으로 예상됩니다. (EMA는 5월2일경, FDA는 5월9일)

PRX102의 파트너는 앞서 말한 Chiesi 인데 연구중심의 제약사이고 연 수입이 30억달러인 빅팜이고 전세계 30개국에 6000명이상 직원이 있는 글로벌 회사, 패브리병에 전문 지식을 가진 재능있는 희귀질환부서를 보유하고 있고, PRX102의 성공적인 상업화를 위한 마케팅조직과 세일즈 조직을 갖추고 있다고 합니다.
10억달러(1조3천억원) 의 마일스톤을 받을 수 있고, 미국에선 15~40%의 로열티, 미국제외한 글로벌엔 15~35%의 높은 로열티를 받을 수 있다고 합니다. (현재 시가총액은 1500억원대 입니다)

현금은 20.8m달러가 있고, 22년도 수익은 21.2m 달러라고 합니다.하지만 부채가 28.7m 정도 있고, 분기당 5.7m 소진하는거 감안하면, 올해 또는 내년 안에 오퍼링 가능성은 있어보입니다.
중요한건 시가총액이죠.
이 슬라이드에선 55.8m (약 730억원)으로 되어 있는데, 현재 기준으론 117.6m (약 1500억원)으로 저때에 비해 2배이상 오른 상태이지만, 여전히 천억원대의 시총으로 매우 낮은 상황입니다.
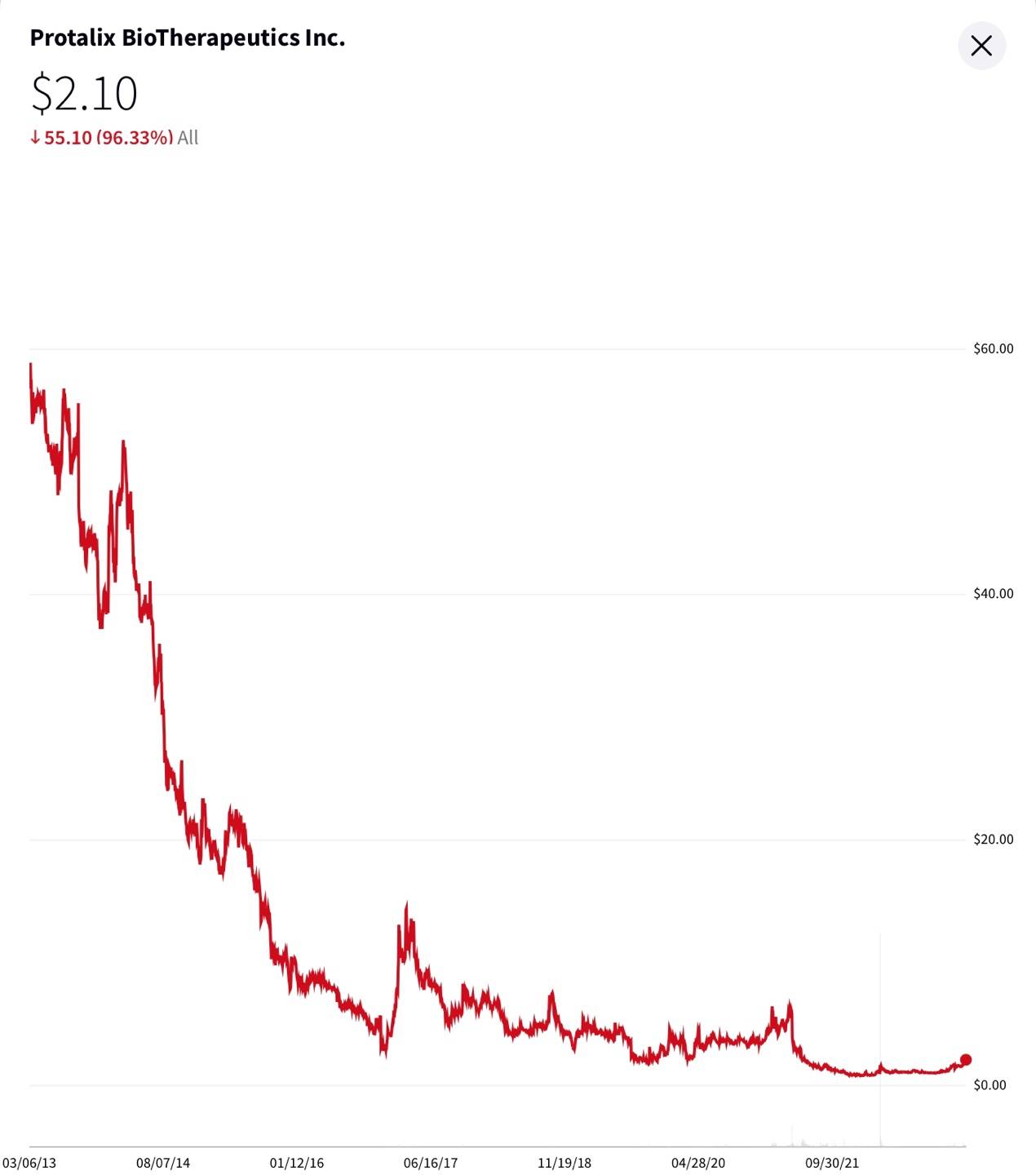
10년전과 비교하면 60불에서 2불로 약 96% 마이너스인 종목이네요.
당시엔 왜저리 높았는지 모르겠는데, 아마도 고셔병 치료제 나오고, 바이오 호황기때의 거품인 것으로 보여집니다.
가장최근 폭락은 20년~21년 사이의 폭락입니다.
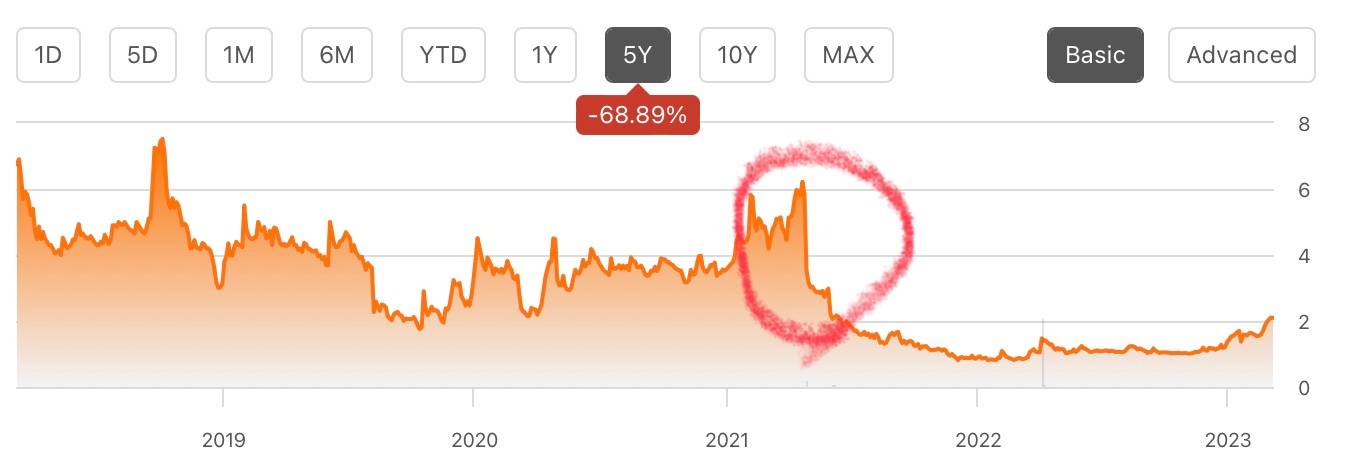
6불에서 1불 쯔음으로 쫙 폭락했는데,
당시 사유는 패브리병 치료제인 PRX-102가 FDA로부터 CRL을 받았기 때문입니다.
CRL을 받은 이유는 임상에 문제가 있어서가 아니라, 코로나 상황으로 인한 제조시설 현장실사 불가 때문입니다. (이스라엘에 있어서 불가능했습니다)
RISK
아델릭스도 하반기 엑스포자의 승인결과가 남아있는 것처럼, 유럽 EMA와 FDA에서 승인거절 가능성이 없는 게 아니고, 매출 역시 아델릭스와 비교하면 지난해 출시한 IBSRELA의 매출성장세가 뚜렷하고 시장크기도 좋지만, 프로탈릭스의 고셔병 치료제는 출시된지 오래되었지만 연 20m (250억원)정도에 불가하단 점, 그리고 빠른 자금소진으로 인해 오퍼링 가능성이 있다는 점이 리스크라고 볼수 있을 것 같습니다.
그리고 이미 ATM 오퍼링을 한적이 있는데, 그 물량이 다 나오지 않은 상태로 추정됩니다.
또한 기존치료제에 비해 명확한 장점도 분명히 있긴 하지만, 기존치료제와 비열등성만 입증했을 뿐, 우월한 효과를 입증한 것은 아니란점, IRR(infusion-related reaction)에서 명확한 장점은 있긴 하지만, 그게 승인여부와 직결되는 부분인지에 대한 다소 의문이 있는 부분도 있습니다.
(물론 반대로 얘기하면 이미 시판된 약물과 동등한 효과를 입증하고 더 안전한 약물이라고 볼 수도 있습니다)
마무리
3상 임상 3개를 모두 성공하고, 약효과 무관한 부분으로 CRL 받아서 큰 하락이 있던 회사로서, 곧 다가오는 2개의 catalyst가 있는 회사입니다.
유럽 EMA, 미국 FDA에 승인받으면, 수령할 마일스톤과 매출예상액을 고려한 업사이드에 비해, 현 시점의 시가총액은 저평가구간으로 생각됩니다.
하지만 여전히 승인거절 가능성이 있으며, 자금조달을 위한 오퍼링이 예상되기도 합니다.
PRX 102는 패브리병 치료에 있어서 여러 장점을 보유한 파이프라인으로 시장의 unmet needs를 만족시켜줄 수 있는 잠재력을 가지고 있다고 판단됩니다.

Disclaimer
-저자는 보고서 제공시점 기준 일부 보유하고 있어 편향된 시각일 수 있습니다.
-당사는 모든 컨텐츠는 저작권법의 보호를 받은바, 무단 전재, 복사, 배포를 금합니다.
-콘텐츠에 수록된 내용은 개인적인 견해로서, 당사 및 크리에이터는 그 정확성이나 완전성을 보장할 수 없습니다. 따라서 어떠한 경우에도 본 콘텐츠는 고객의 투자결과에 대한 법적 책임소재에 대한 증빙 자료로 사용될 수 없습니다.
-모든 컨텐츠는 외부의 부당한 압력이나 간섭없이 크리에이터의 의견이 반영되었음을 밝힙니다.
Disclaimer
- 당사의 모든 콘텐츠는 저작권법의 보호를 받은바, 무단 전재, 복사, 배포 등을 금합니다.
- 콘텐츠에 수록된 내용은 개인적인 견해로서, 당사 및 크리에이터는 그 정확성이나 완전성을 보장할 수 없습니다. 따라서 어떠한 경우에도 본 콘텐츠는 고객의 투자 결과에 대한 법적 책임소재에 대한 증빙 자료로 사용될 수 없습니다.
- 모든 콘텐츠는 외부의 부당한 압력이나 간섭없이 크리에이터의 의견이 반영되었음을 밝힙니다.