ivr의 팜
네오이뮨텍(950220)-사업화 시점의 사정권 진입

IV리서치
2025.07.06
기업개요
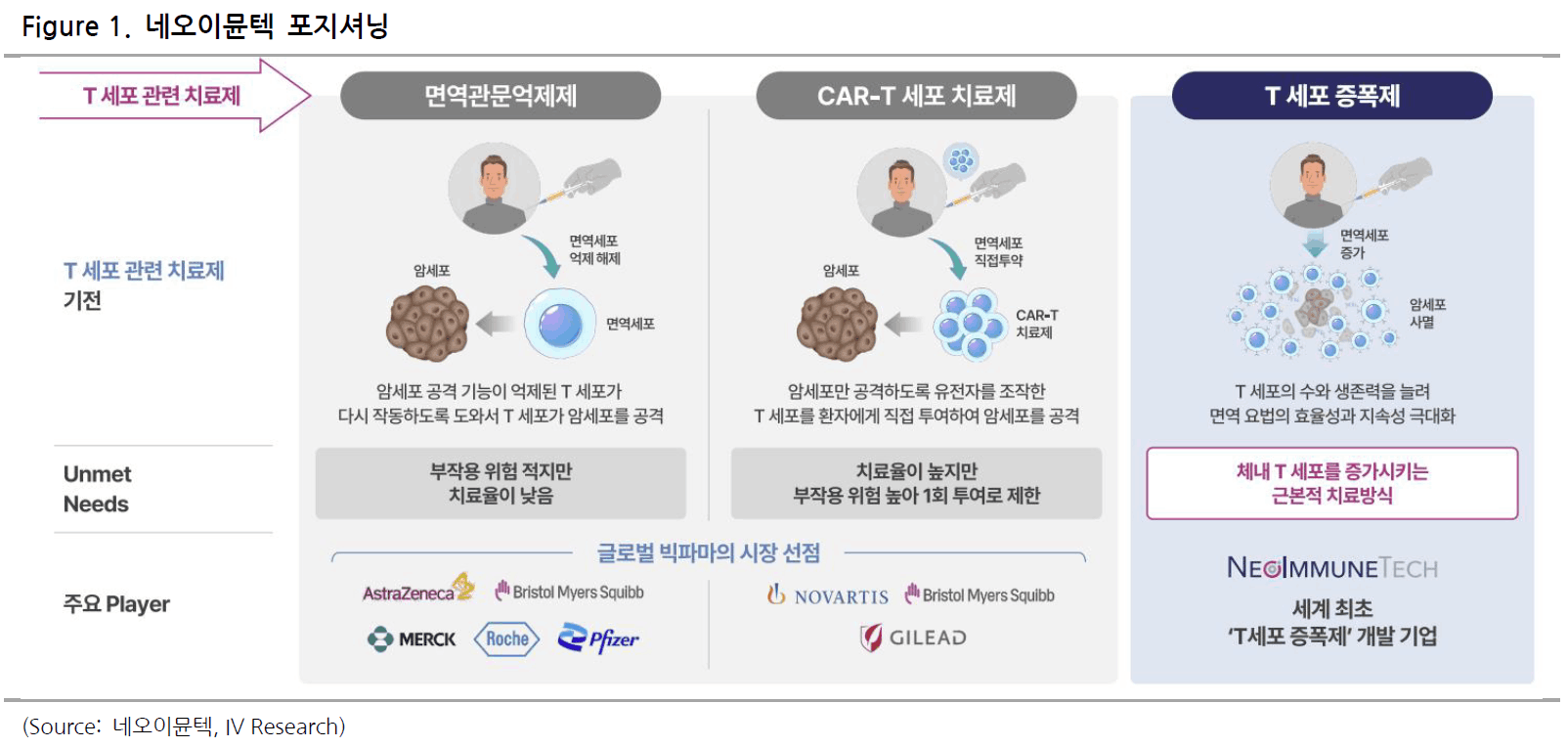
동사는 T세포 기반 면역치료제를 개발하는 신약 바이오 벤처기업으로, 핵심 파이프라인 NT-I7은 인체 CD4·CD8 T림프구를 선택적으로 증식시키는 차세대 T세포 증폭제이다. 기존 면역관문억제제, CAR-T의 한계를 보완해 지속적이고 균형잡힌 T세포 풀을 재구성함으로써 항암면역 효율을 극대화한다. 동사의 사업전략은 NT-I7을 축으로 ‘T세포 증폭 플랫폼’ 생태계를 구축하는 것이다. 초기에는 단독 투여 및 방사선 사고 대응용 ARS 적응증으로 시장에 진입하고, 중장기적으로는 다양한 면역항암제, 세포치료제와의 병용을 통해 파이프라인을 다각화하는 전략이다. 동사의 최대주주는 코스닥 상장사 제넥신으로 지분율 21.18%를 보유 중이다.
ARS(Acute Radiation Syndrome, 급성 방사선 증후군) 치료제
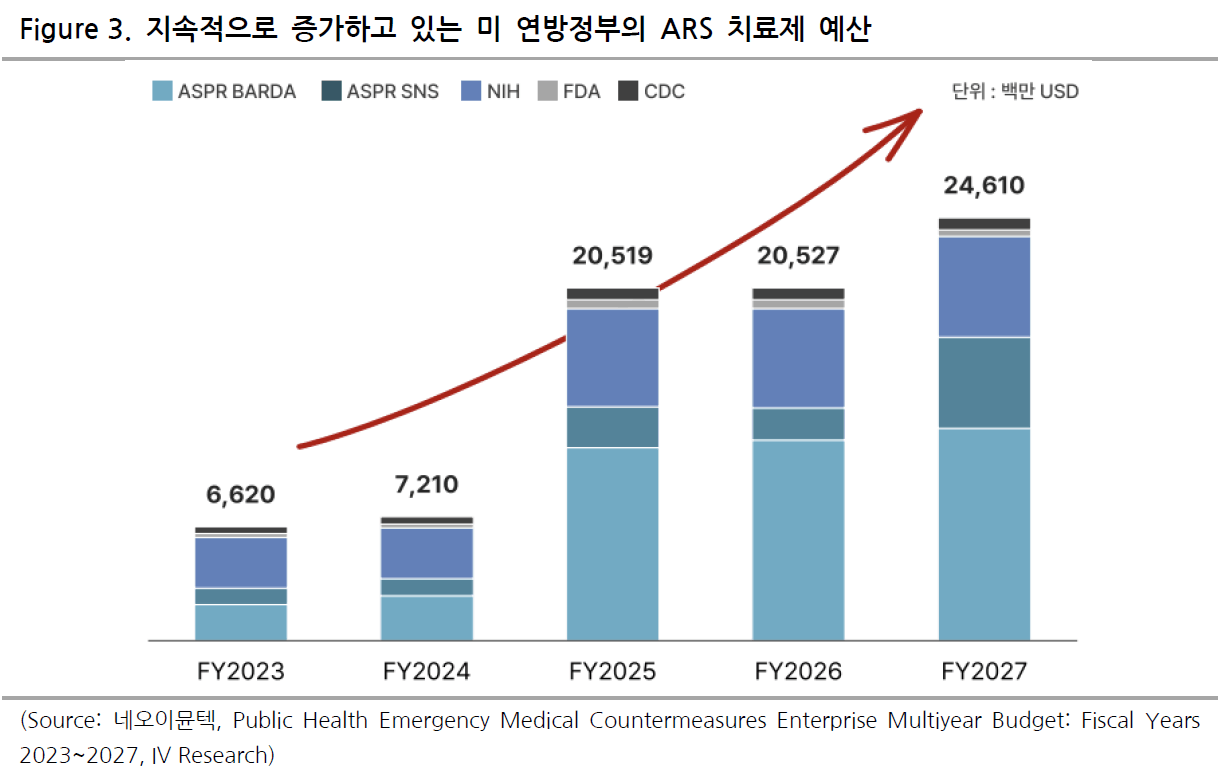
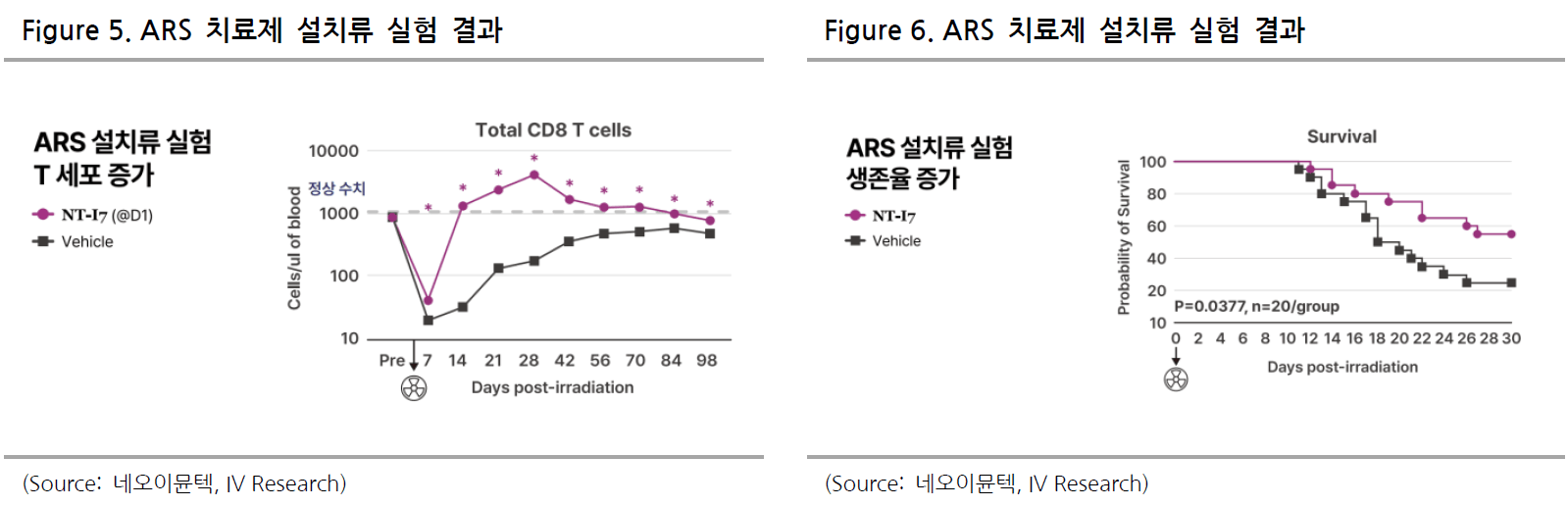
급성방사선증후군(ARS)은 1 Gy 초과 방사선 노출로 골수 억제와 림프구 고갈이 동반되는 치명적 상태를 의미한다. 미국 정부는 생물테러, 원전 사고 대비 차원에서 BARDA, SNS 예산을 확충하며 전략적 비축을 추진하지만, 림프구 복원제를 아직 확보하지 못한 상황이다. NT-I7은 이 공백을 메울 유일한 T림프구 증폭제로 First-in- Class 지위를 노린다. 2024회계연도 BARDA 운용예산은 전년 대비 30% 증가하여 NT-I7 도입 가능성을 높이고 있다. 동사와 듀크대의 공동 비임상 결과는 정부 조달의 과학적 근거를 제공한다. 2024년 8월 NIAID 설치류 모델에서 T세포 복원 및 30일 생존율 60%를 달성해 Vehicle 대비 세 배 향상을 입증했다. 영장류 시험은 2024년 12월 개시, 4Q25 종료 예정이고 중간 분석은 3Q25 학회를 통해 소통이 예상된다. 초기 결과가 지속적으로 유지되는 경우 2026년 FDA Animal Rule 경로로 BLA 제출이 가능하며, 승인 후 BARDA 조달을 통해 연간 약 1,000억 원 매출이 예상된다.
CAR-T 치료제와 병용투여 임상 진행 중
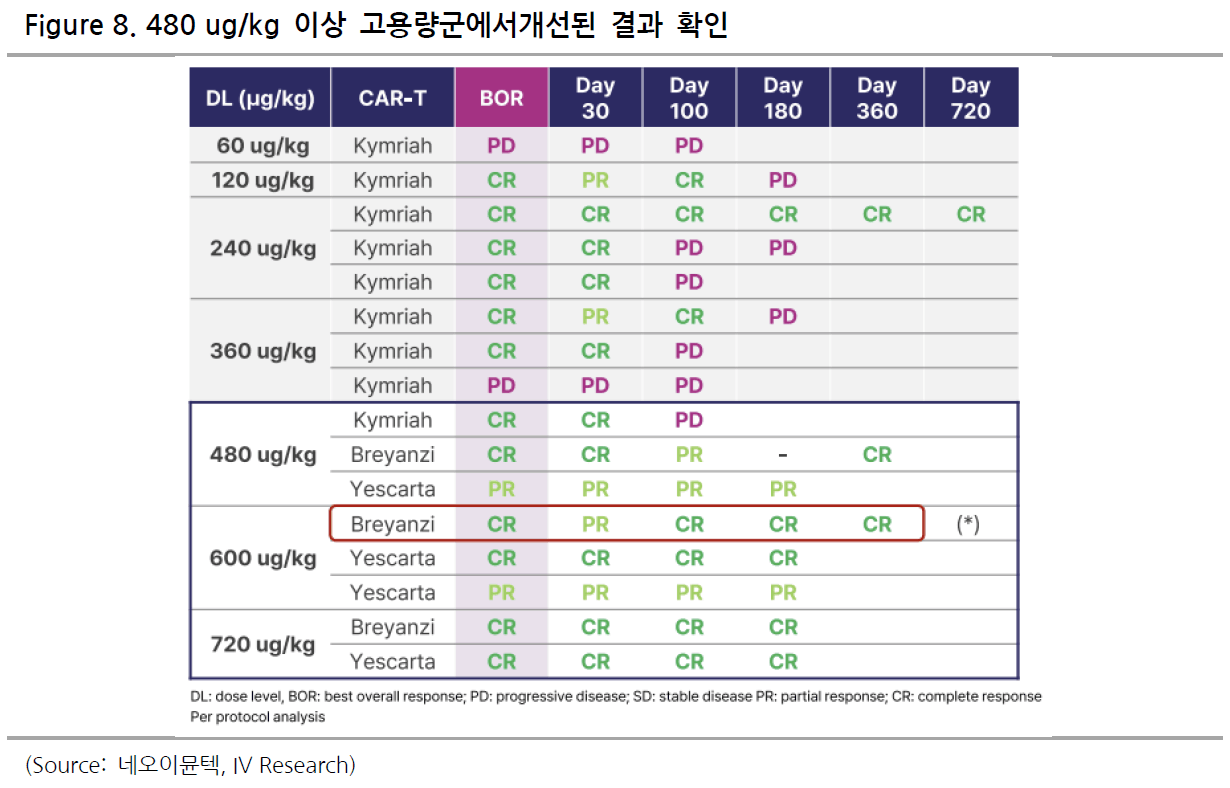
CAR-T 치료제는 혈액암에서 높은 초기 반응을 보이지만, 투여 횟수 제한과 조기 T세포 고갈로 인해 지속성이 떨어진다는 단점을 갖는다. NT-I7은 CAR-T 투여 후 10–21일 사이에 병용투여 함으로써 체내 잔존 CAR-T 세포를 재증식시켜 치료 내구성을 강화할 수 있다. 이는 IL-7 특유의 선택적 T세포 증폭과 향상된 반감기를 활용해 사이토카인 폭풍, 신경독성 같은 급성부작용 없이 CAR-T 용량을 재충전하는 신규 기전으로 평가된다. 2025년 5월 확보된 Topline 데이터에 따르면 480 µg/kg 이상 투여군에서 완전관해율 75%(6/8), 6개월 전체반응률 88%(7/8)를 기록했다. 투여 21일 후 CAR-T 세포 수가 급증해 90일까지 검출이 가능했으며, Grade 3 이상 NT-I7 관련 이상사례, 사이토카인 폭풍, 신경독성 등은 보고되지 않았다. 브레얀지, 예스카타, 킴리아 등 주요 CAR-T 치료제의 초기 유효성 데이터를 상회하는 결과로, 동 데이터 발표 이후 글로벌 제약사와 기술이전 협상이 진행 중인 것으로 파악된다. 향후 프로토콜 조정으로 10일차 조기 투여로 변경하여 반복투여 효과를 극대화할 계획이다.
댓글 0

첫번째 댓글을 남겨주세요