웰쓰빌더의 프리미엄 리포트 :)
알테오젠 아일리아 바이오시밀러 유럽 품목 허가 획득(Feat. 비만치료제도)

웰쓰빌더
2025.09.17

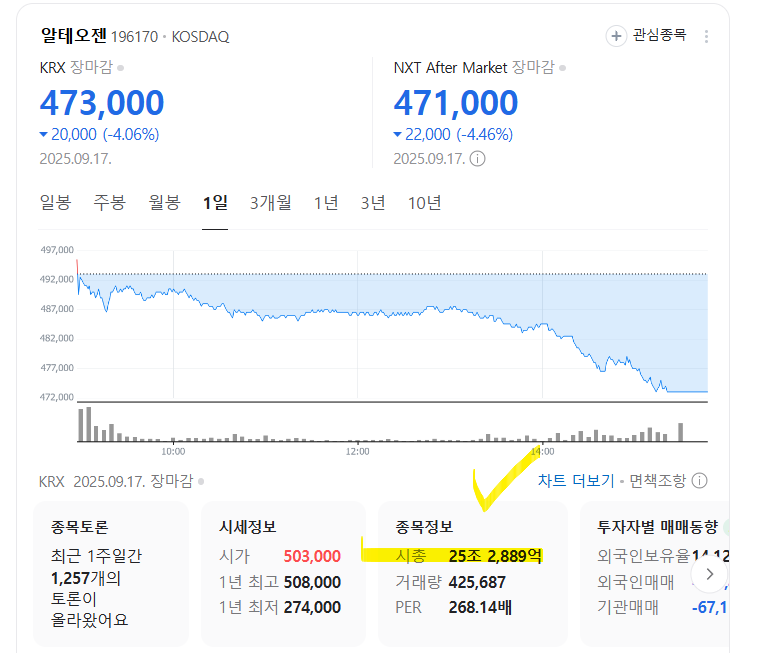
알테오젠 주가가 무려 4%나 하락했다.
시총은 현재 25조.
50만원을 뚫냐 마냐의 싸움이었는데
9월 23일 키트루다SC FDA승인이 나오기 전에
크게 오르지 않는 것이 조금 아쉽다.
본문 핵심만 요약하면

알테오젠은 아일리아 바이오시밀러 '아이럭스비'의 유럽 품목허가를 획득하며 글로벌 시장 진출에 성공했다.
피하주사 전환 플랫폼 ALT-B4를 통해 다수 글로벌 제약사와 기술이전을 진행 중이며, 추가 본계약도 기대된다.
한 달 지속형 비만치료제 개발과 키트루다 SC FDA 승인 기대감이 주가에 중장기 모멘텀으로 작용할 전망이다.
박순재 대표님께서..
2-3년 내에 7건이 또 본계약 체결 가능성이 있다니
정말 대단하다.
알테오젠 아이럭스비
유럽 품목허가 획득은?


알테오젠, 아일리아 바이오시밀러 ‘아이럭스비(Eyluxvi®, ALT-L9)’ 유럽 품목 허가 획득
승인 기관: 유럽연합 집행위원회(EC)
제품: 아일리아® 바이오시밀러 ‘아이럭스비’ (ALT-L9)
적응증:
습성 연령관련 황반변성(wAMD)
망막정맥폐쇄성 황반부종(BRVO/CRVO)
당뇨병성 황반부종(DME)
근시성 맥락막 신생혈관(myopic CNV)
의미:
알테오젠이 자체 물질 도출 및 임상 개발을 주도한 첫 바이오시밀러 제품
허셉틴 바이오시밀러(중국 치루제약 유통)에 이은 두 번째 허가 제품
유럽 상업화를 위한 파트너십 추진 중
임상 근거:
2022년 6월~2024년 2월, 12개국에서 431명 대상 임상 3상
오리지널 아일리아 대비 동등한 효능 및 안전성 입증
아일리아 바이오시밀러 ‘아이럭스비’가 유럽 판매 승인을 획득하며 글로벌 진출 기반을 마련했음.
오리지널과 동등한 효능·안전성을 입증한 글로벌 임상 결과로 제품 신뢰도를 확보했고
유럽 상업화를 위한 파트너십을 추진 중이며, 블록버스터 시장 진입으로 매출 성장 기대가 크다.
비만약까지?
오늘 코리아 인베스트먼트위크 2025에서
박순재 알테오젠 대표님이 나오셨다.

*대략적으로 비만치료제 관련해서
내용을 보자면..
알테오젠은 부작용을 낮추고 약효를 한 달간 유지하는 장기지속형 비만치료제를 개발 중이며, 2027년 임상 진입 목표를 세웠다.
‘퓨전 테크놀로지’ 기반의 월 1회 제형은 기존 주 1회 약물(위고비, 마운자로) 대비 차별화된 경쟁력을 갖는다.
한 달에 한 번 투여하는 비만 치료제를 개발 중으로, 2027년 임상 개시를 목표로 삼고 있다는 것이 포인트
근데 이번에 KIW에서 박순재 대표님께서 말한 내용이 있다.
ALT-B4는 IV(정맥주사) 제형을 SC(피하주사)로 전환하는 알테오젠의 핵심 플랫폼이다.
이미 MSD, 다이이찌산쿄 등 6개 글로벌 제약사에 기술이전 완료.
10여 개 기업과 추가 협의 중이며, 이 중 최대 7건이 2~3년 내 본계약 체결 가능성이 있다.
최대 7건이라는 것이 포인트...
알테오젠은 아이럭스비 유럽 품목허가를 통해 글로벌 바이오시밀러 시장 진입에 성공했고,
비만 치료제와 ALT-B4 플랫폼 기반 기술수출로 추가 성장 모멘텀도 확보한 상태임
9월 23일 예정된 키트루다 SC FDA 승인 결과가 주가 방향성의 핵심 변수가 될 전망임.
단기 조정에도 불구하고, 중장기 성장성도 기대된다.
댓글 0

첫번째 댓글을 남겨주세요
